
Естери. Жири
Реакція взаємодії спирту з кислотою в результаті якої утворюється речовина естер та вода, називається реакцією естерифікації.

Реакція естерифікації відбувається в присутності каталізатора та при нагріванні. Зазвичай каталізаторами слугують сильні неорганічні кислоти. Під час естерифікації від молекули кислоти від'єднується група —ОН, а від спирту - Н. Об'єднуючись вони утворюють молекулу води. "Місточком" між замісниками кислоти та спирту є атом Оксигену, що залишився у молекулі спирту. Речовина СН3СООС2Н5 і є наш естер.
Реакція естерифікації є оборотною (рівноважною). Процес, зворотний до естерифікації — гідроліз (в присутності лугу - омилення).

Що ж це за речовини естери? Естери це речовини, що мають два вуглеводневі радикали (замісники), пов'язані між собою групою атомів —СОО—, їх загальну формулу можна зобразити так: R—COO—R'
Для того щоб правильно назвати естер, треба звернути увагу на радикали (замісники). У наведеному рівнянні реакції видно, що перший радикал R - це залишок оцтової кислоти, а другий R'- залишок етилового спирту. Називати естери починаємо з R'. Отже — етиловий естер оцтової кислоти або етилацетат (етилетаноат).
Фізичні властивості естерів: більшість естерів рідини, що легші за воду та нерозчинні у ній. Естери нижчих карбонових кислот мають приємний фруктовий чи квітковий аромат. Тому їх використовують як штучні ароматизатори у парфумерії, кондитерській справі, виготовленні солодких напоїв тощо. Наприклад: бутилацетат (бутилетаноат) має аромат груш (хто з нас не любить цукерочки "Дюшес"?☺), метиловий естер масляної кислоти надає запаху яблукам, етилсаліцилатом пахне м'ята.
Запитаєте, а до чого тут жири?☺ Відношення безпосереднє.
Жири це естери вищих жирних карбонових кислот та трьохатомного спирту гліцеролу.
Формули цих кислот:
пальмітинова (гексадеканова) С15Н31СООН,
стеаринова (октадеканова) С17Н35СООН, олеїнова (октадеценова) С17Н33СООН

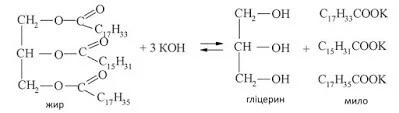
Під час гідролізу жирів утворюється гліцерол та вищі карбонові кислоти. А в результаті гідролізу (омилення) жирів у присутності лугу добувають різні види мила і гліцерол. Натрієві солі дають тверде мило, а калієві — рідке.
Докладніше про властивості та застосування жирів
моїм студентам потрібно розглянути самостійно.
Домашнє завдання: підручник Попель, Крикля для 10
класу: § § 21, 22, вправа 149 сторінка 124, вправа 167 сторінка 135. Зробити
конспект.
Виконуєте в робочих зошитах Лабораторну роботу №2 "Ознайомлення зі зразками естерів. Дослідження фізичних і хімічних властивостей жирів."
Відповіді розміщуєте на стінці Padlet.
Готуєтеся до усних відповідей за даною темою.






